科普中国头条推送

2019年未来科学大奖生命科学奖获奖人——邵峰
从细菌中获得的创新启示
用未来科学大奖科学委员会的成员何川教授的话来说,这一奖项最亮眼的点就是两个字:创新。虽然从文字上看,我们很难理解这些专业术语。但在人类漫长的演化史中,人体已经对这一套生理机制驾轻就熟。而直到近些年,邵峰首创性地发现了这一系列免疫机制,将细菌与人类的错综复杂的另一层关系展示在科学界面前。
之所以说人和细菌的关系复杂,那是因为人本身就是和无数细菌共存的,有些细菌能够给人带来好处,比如大肠杆菌可以维持肠道健康,并合成一些人体所需的维生素和物质。但有些细菌却会让人患上疾病,对人体有害,比如金黄色葡萄球菌会产生肠道毒素,造成急性感染症状。为此,人类在演化过程中也产生了许多防卫机制,用于阻挡和识别细菌种类。
在人体中,如果细菌想要进入细胞,首先就要通过细胞膜。而细胞膜上的一些蛋白能够识别细菌,向细胞发出“警告”信号,以此来激活免疫系统,抵抗细菌。这是人类在与细菌博弈中一种很关键的防御机制。因此,有许多科学家一直在尝试鉴定和分析,细胞膜上有哪些蛋白,或者说受体与细菌侵入有关。
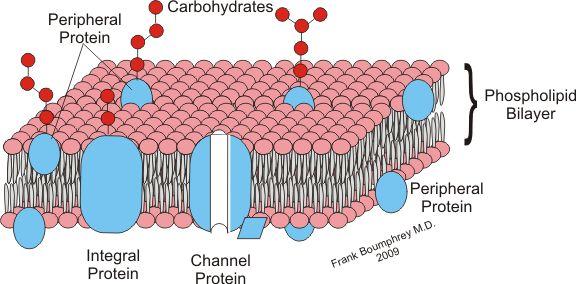
细胞膜表面有许多膜蛋白(蓝色),在识别外来入侵细菌中有重要作用。但邵峰跨越了这层膜,把视野投向了细胞
一直以来,与细菌识别相关的膜蛋白都属于比较热门的研究方向。不过,邵峰没有选择跟随大流,在其他人专注于研究细胞膜上的识别蛋白时,他将自己研究的视野放到了一个更深的层次,也就是细胞内部发生了什么。
开辟天然免疫和细胞焦亡新方向
邵峰告诉我们,其实他一开始从事的是细胞毒素方向的研究,并且已经发了不少高质量的论文。但美中不足的是,这一研究方向的涉及科学问题比较窄,只能供一个很小领域的人来讨论。而他想要做出可以供大多数科学家都能够欣赏,具有借鉴价值的成果。因此他决定走出原本的舒适圈,转向了天然免疫的研究方向,大胆假设之后,他决定去寻找胞内细菌识别受体,走一条前人还没怎么走过的路。
这种科学上的大局观和见解的独到性,也让邵峰发现了其他人都没有触及的细胞秘密,也就是获奖理由中提到的:识别LPS的受体和执行蛋白。LPS指的是革兰氏阴性菌细胞壁的脂多糖,这些脂多糖是细菌的标签,也是细胞来区分细菌是敌是友的标志物。而邵峰的一系列研究,揭示了人体细胞内部是用什么蛋白来识别LPS,即细胞是如何识别细菌的天然免疫机制。
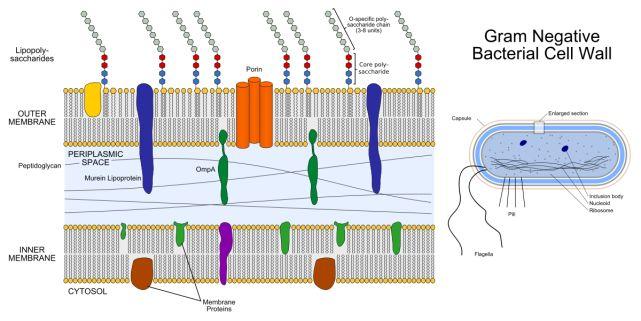
革兰氏阴性菌表面会有许多LPS(图中表面成串结构),右边为细菌模式图。图片来源:Wikipedia
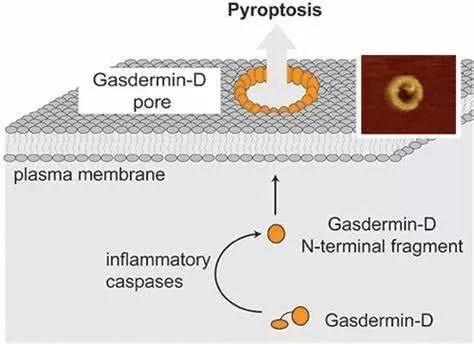
打孔蛋白D(Gasdermin-D)能够通过在细胞表面打孔,并引起细胞焦亡(Pyrotosisi)。图片来源:University of Basel
研究结果具有潜力无限的临床价值
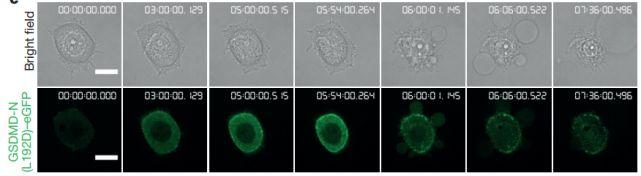
邵峰在2016年发表的文献中,就展示了gasdermin蛋白在细胞焦亡过程中在细胞中的定位和作用。图片来源:Pore-forming activity and structural autoinhibition of the gasdermin family
用邵峰自己的话来说,发现细胞内部的识别受体,以及细胞焦亡的这一系列重要机制,就有望从细胞焦亡和天然免疫系统入手,调节炎症反应,改变免疫微环境。这些既包括正常细胞的微环境,也包括肿瘤细胞的微环境。如今,邵峰多年的工作积累已经找到了许多引起细胞焦亡的上游蛋白受体,这意味能利用这些新的靶点来开发药物。比如由于LPS受体过度激活,引起了细胞焦亡不正常地发生,最终可能引起败血症。这一过程中,gasdermin D过度活化是至关重要的,因此药企和生物技术公司可以针对gasdermin D开发药物来治疗败血症。
对于何时能从这一系列的天然免疫中,真正开发出临床应用的药物或者疗法。邵峰有着自己的见解,他认为基础研究最终走向临床应用,这应该是每一个做基础研究的科学家都努力追求做到的,也是研究者的终极目标。“我在三、四年前就有这方面的工作计划,有一些公司也在尝试筛选一些小分子药物,尤其是针对gasdermin蛋白起效的。”不过邵峰告诉我们,他现在暂时还没有把过多精力放在转化方面的研究上,因为他想积累更多有关炎症、天然免疫与细胞焦亡的新发现和知识,来丰富和巩固这一领域的知识框架和体系,这对于未来靶点药物的研发很关键,可以最大程度保证药物研发的努力能够最终成功。
继续用科学改变未来
如今,回国十几年的邵峰,研究团队仍然只保持着不到二十人的规模。他对研究团队成员的要求也如同对自己研究方向一样,那就是在科学态度上要有最大的坚持、在科学思路上要有缜密的逻辑。邵峰坦言自己2005年回国到2010年这段时间,也曾迷茫过。一边是细菌毒素方面的研究成果不断发表在《科学》等顶级学术期刊上,另一边是现实与理想的科研目标之间仍然有不小的距离。最终他选择了坚持理想,踏进了天然免疫研究的圈子。这些年的坚持和他所说的线性化研究也让他收获了这一次的未来科学大奖。

2019年未来科学大奖科学委员会骆利群(右一)和庄小威(右二)分别用中英文宣读获奖人以及获奖理由
在未来论坛的现场连线中,当邵峰得知自己获奖时,表现得异常平静,第一句回复也只有简单的三个字“挺好的”。在会后的采访中,邵峰表示他自己的激动点其实非常高。但在撰写和投递天然免疫研究的文章时,会格外的高兴。而如今,这样一位冷静的科学家在未来还将给我们带来更多的改变,因为他刚下飞机,就兴奋得赶往实验室整理即将投递的两篇论文。就如同上一届获奖者带给我们的科学魅力,邵峰也正在以自己的方式,用科学改变未来。
采访人| 栗琳 未来论坛青年理事、清华大学生命科学学院研究员、助理教授,以及豪思生物创始人
受访人| 邵峰 中国科学院院士、北京生命科学研究所学术副所长、资深研究员;本文在发布前由邵峰老师本人审核
撰稿人| 杨心舟
文章由腾讯科普“科普中国头条创作与推送项目”团队推出
转载请注明来自科普中国